Engineered immunosuppressive dendritic cells protect against cardiac remodelling
病理性心脏重构以慢性炎症和进行性间质纤维化为特征,是导致心力衰竭(HF)的核心驱动因素,也是全球范围内的主要死因。虽然炎症反应在初期具有适应性,但其持续存在会导致不可逆的心肌损伤。目前的治疗策略,包括全身性免疫抑制剂和单一细胞因子抑制剂,往往因脱靶效应和心脏炎症复杂的性质而效果有限。近日,发表在《自然》(Nature)杂志上的一项里程碑式研究揭示了一种新型免疫治疗平台:工程化免疫抑制性且靶向纤维化的树突状细胞(iCDCs),该平台通过局部、多维度的免疫重编程来保护心脏。
iCDC平台的构建
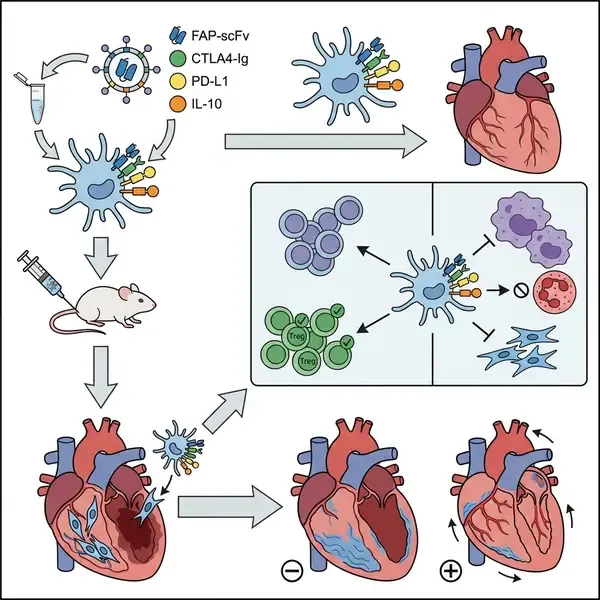
树突状细胞(DCs)是连接先天免疫和适应性免疫的专业抗原提呈细胞。为了利用其在心脏修复中的潜力,研究团队对骨髓来源的DCs进行了工程化改造,使其表达一种类似嵌合抗原受体(CAR)的结构。该结构包含一个针对成纤维细胞激活蛋白(FAP)的单链抗体片段(scFv),FAP在受损心肌的活化成纤维细胞中高度表达。为了确保强效且稳定的免疫抑制,iCDCs还被装备了组成型表达的三种关键调节因子:CTLA4-Ig、PD-L1和IL-10。这种设计使iCDCs能够特异性地归巢至纤维化病灶,并在不引起全身免疫抑制的情况下抑制病理性免疫回路。
多种疾病模型中的治疗效果
研究人员在多种小鼠模型中评估了iCDC疗法,包括心肌梗死(MI)、缺血再灌注(I/R)损伤和横向主动脉缩窄(TAC)诱导的压力负荷模型。在所有模型中,静脉注射iCDC(最佳时间为损伤后第3天)均显著减轻了心脏纤维化并保留了收缩功能。值得注意的是,iCDC疗法提高了左心室射血分数(EF)和缩短分数(FS),增强了新生血管形成,并延长了晚期心力衰竭小鼠的生存期。研究表明,FAP靶向scFv与三重调节因子载荷的完整组合是实现这些治疗效益的必要条件。
机制解析:免疫与基质重编程
通过整合大块组织和单细胞RNA测序(scRNA-seq),团队解析了iCDC介导心脏保护的机制。他们发现iCDC通过双重路径发挥作用: 1. T细胞调节: iCDC抑制促炎性T细胞亚群(如Th17和效应记忆T细胞)的活化,同时促进组织驻留调节性T细胞(Tregs)的持久克隆扩增。这些Tregs表现出增强的活化和生存标志物,促进了长期的免疫稳态。 2. 髓系与基质重编程: 除T细胞外,iCDC还直接重构了更广泛的心脏微环境。它们使巨噬细胞群体从促炎性CCR2+亚群转向修复性TIM4+组织驻留表型。此外,iCDC抑制了中性粒细胞和B细胞的活化,并直接抑制成纤维细胞的致纤维化活性,在不产生直接清除成纤维细胞风险的前提下减少了细胞外基质沉积。
非人灵长类动物的转化验证
该研究的一个关键亮点是在食蟹猴心梗模型中验证了iCDC疗法。心梗后给予自体iCDC导致心脏功能持续改善(通过超声心动图和MRI测量)、梗死面积缩小以及心肌灌注增加。全面的安全性评估(包括连续心电图监测和主要器官的组织病理学分析)未发现心律失常、全身毒性或不良免疫反应的证据。这一在非人灵长类动物上的成功转化,突显了iCDC作为人类心力衰竭安全有效疗法的临床潜力。
科学价值与未来展望
这项研究通过从广泛的免疫抑制转向局部的、基于细胞的免疫重编程,引入了心力衰竭治疗的范式转变。与依赖细胞毒性清除成纤维细胞(可能损害结构完整性)的CAR-T或CAR-巨噬细胞疗法不同,iCDC通过对整个炎症生态位的非细胞毒性调节来实现治疗效果。通过整合空间靶向与多靶点免疫抑制,iCDC提供了一种精密且持久的策略来阻断心脏重构,为未来再生心脏病学的临床试验奠定了坚实基础。