Accelerating discovery of cancer causes for prevention in the era of rising early-onset cancers
全球肿瘤学格局正在发生深刻变化。癌症曾被视为老年病,但现在50岁以下成年人的发病率正迅速上升。这种早发性癌症的激增,特别是在X世代和千禧一代中表现出的显著“出生队列效应”,促使科学界对癌症病因的发现和预防策略进行重新审视。在《细胞》(Cell)杂志发表的一篇里程碑式前瞻性文章中,一个国际研究团队提出了加速癌症病因发现的全面蓝图,倡导从静态的流行病学“快照”转向动态的、生命历程整合的研究框架。
早发性癌症激增的危机
来自42个国家的数据显示,75%的地区在年轻人中观察到至少六种癌症(包括结直肠癌、乳腺癌和子宫内膜癌)的发病率上升。尽管老年人群的癌症死亡率有所下降,但年轻人群的死亡率却处于平台期甚至有所上升。这一转变表明,当代人比前几代人更早地接触到更复杂、更普遍的致癌暴露。然而,目前的模型仅将30%–45%的癌症归因于已知的可改变因素,而理论上高达80%的癌症是可以预防的。这一差距凸显了现有研究在捕捉“暴露组”(从受孕到死亡的总暴露)及其在关键发育窗口期产生的生物学后果方面的不足。
超越“黑箱”:整合机制与人群科学
从历史上看,癌症病因的发现遵循两条路径:流行病学的“黑箱”法(识别关联)和机制生物学(实验室测试)。虽然这些方法成功识别了烟草和肥胖等主要风险,但在应对早发性癌症时已显疲态。作者指出,早发性癌症的兴起不太可能仅由生殖系遗传解释,因为等位基因频率的变化非常缓慢。相反,遗传易感性更可能作为现代环境损伤的调节因子发挥作用。
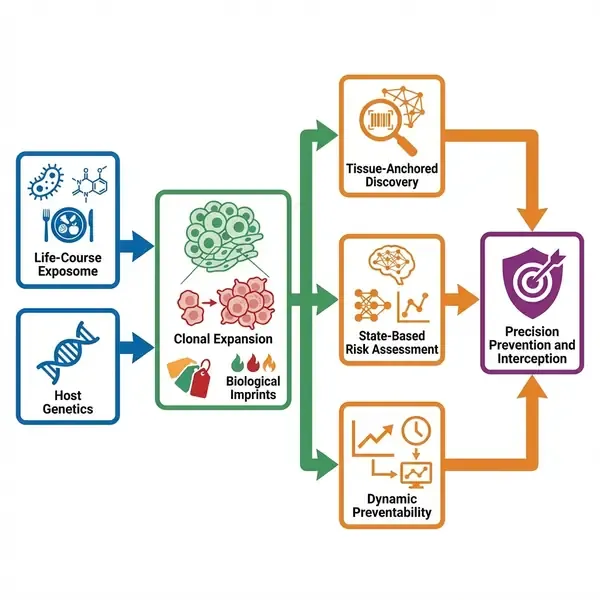
为了弥补这一差距,研究人员提出了三个互连的框架:
1. 以组织生态系统为锚点的框架: 该框架将癌症风险重新定义为动态组织生态系统的涌现属性。它关注“组织记忆”——即由短暂暴露(如感染、饮食)留下的持久生物学印记,这些印记通过表观遗传重编程、免疫转变和突变特征进行编码。一个典型的例子是结直肠癌中与大肠杆菌素(colibactin)相关的突变特征,该特征在早发性病例中更为普遍,提示早年接触特定产毒细菌可能是致病因素。
2. 基于生物状态的精准风险评估框架: 超越了Gail模型等静态工具,该框架利用纵向电子健康档案(EHR)和多组学数据。通过将人工智能应用于连续的临床数据(如重复的乳腺摄影或EHR中的疾病轨迹),研究人员可以实时识别进入高风险生物状态的个体,从而实现定制化的筛查和“免疫拦截”策略。
3. 癌症可预防性的动态框架: 传统的人群归因分值(PAF)通常假设各因素相互独立,且忽略了风险降低的时间过程。提议的动态框架使用微观模拟模型(如CISNET),整合特定出生队列的暴露轨迹和癌症自然史。这使得科学家能够真实地预测干预措施(如GLP-1受体激动剂的广泛使用或控烟政策)对未来癌症负担的影响。
克服资源与方法学障碍
该蓝图识别了重大障碍,特别是数据的碎片化。由于早发性癌症在绝对数量上仍相对较少,单一队列往往缺乏快速发现所需的统计效力。作者呼吁建立一个全球连接的生态系统,通过联邦学习和统一标准来整合现有的队列、EHR和生物样本库。此外,他们强调需要开发能够处理多模态、纵向数据的高级因果推断方法,以区分时间依赖性混杂因素与真正的中介效应。
未来预防的愿景
文章最后指出,早发性癌症的上升是慢性病流行病学更广泛转变的预兆,包括糖尿病和心血管疾病的发病提前。通过关注共同的系统性破坏和组织层面的“记忆”,科学界可以迈向整合的预防模式。这一蓝图不仅是加速癌症病因发现的策略,更是对持续基础设施投资和跨学科协作的号召,旨在保护未来一代免受早发性恶性肿瘤日益沉重的负担。