Functional integration of an autologous engineered esophagus in a large-animal model
食管环形缺损的重建一直是再生医学领域的一大难题,特别是对于患有长段型食管闭锁(LGEA)的儿科患者。目前的临床标准通常涉及胃或结肠代食管术,但这些方法伴随着运动功能障碍和移植物失效等长期并发症。在《自然-生物技术》(Nature Biotechnology)发表的一项里程碑式研究中,研究人员展示了自体组织工程(TE)食管在生长中的大动物模型中的成功功能整合,这标志着向临床转化迈出了重要一步。
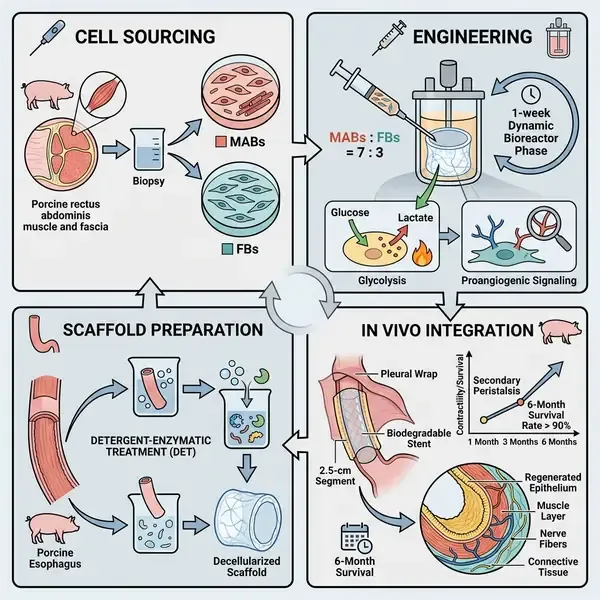
研究团队开发了一套综合策略,利用脱细胞猪食管支架,在保持结构完整性的同时提供器官特异性细胞外基质(ECM)。这些支架通过高密度微注射自体周细胞样生肌前体细胞(中胚层血管母细胞,MABs)和成纤维细胞(FBs)进行细胞回植,这些细胞源自简单的肌肉活检。该流程的一个关键环节是在动态流生物反应器中进行为期一周的成熟培养。单核RNA测序(snRNAseq)显示,这种预处理诱导了接种细胞的代谢转换,使其具备低氧存活能力,并上调了促血管生成通路(如VEGFA、HIF1A),这可能促进了植入后的早期新生血管形成。
研究人员将工程化构建体(长度为2.5厘米)移植到10公斤重的幼猪体内,以模拟儿科应用。手术采用单阶段胸腔移植,辅以血管化胸膜包裹和内部生物可降解支架。研究报告显示,30天存活率为100%,63%(5/8)的动物达到了预设的6个月终点。虽然观察到上皮息肉和吻合口狭窄等术后并发症(这与人类食管手术的临床结果相似),但这些均通过内镜干预得到了成功处理。至关重要的是,实验动物保持了正常的生长曲线,并在无需补充喂养的情况下实现了肠道自主进食。
6个月时的多模态分析为组织再生提供了有力证据。空间转录组学(ST)和组织学评估证实,移植物逐渐恢复了原生食管的结构,包括成熟的复层鳞状上皮形成,以及有组织的黏膜肌层和固有肌层的发育。该研究独特地展示了移植物内平滑肌和骨骼肌表型的出现,并得到了神经再生(β3-tubulin阳性结构)证据的支持。功能恢复通过高分辨率阻抗测压(HRIM)得到了确认,该技术检测到了跨越工程段的继发性蠕动,且离体收缩实验显示移植物对电刺激和化学刺激具有分级反应。
这项研究代表了组织工程环形食管移植物首次在大动物模型中实现支架独立、持续收缩和结构成熟。通过将生产周期(8周)与LGEA修复的临床窗口相对接,并利用自体细胞避免免疫抑制,这种综合再生策略为传统的器官移位术提供了一种极具前景的替代方案,有望改变复杂食管疾病的临床治疗标准。