Exposed phosphatidylserine is an inhibitory molecule in T cell exhaustion
在癌症免疫学和慢性病毒感染研究领域,T细胞耗竭的范式长期以来一直由PD-1、TIM-3和LAG-3等蛋白质抑制性受体的持续表达所定义。然而,由埃默里大学研究团队在《自然》(Nature)杂志上发表的一项开创性研究,将这一框架扩展到了脂质代谢领域。该研究确定了磷脂酰丝氨酸(PS)——一种传统上与凋亡细胞“吃我”信号相关的磷脂——是一种“非经典”抑制分子。它在活的、耗竭的CD8 T细胞表面主动外露,从而抑制免疫反应。
在健康细胞中,PS通常被隔离在质膜的内层,其出现在外层被视为程序性细胞死亡的标志。利用淋巴细胞性脉络丛脑膜炎病毒(LCMV)模型,研究人员证明,虽然T细胞激活会诱导PS的瞬时外露,但慢性抗原刺激会导致耗竭的CD8 T细胞表面持续且高水平地暴露PS。至关重要的是,这些PS阳性细胞保持着生命力且非凋亡,这由缺乏裂解的caspase-3以及它们在重新转移到新宿主后能够存活和增殖的能力所证实。脂质组学和转录组学分析进一步证实了这一发现,揭示了耗竭T细胞亚群中PS生物合成途径(如Ptdss1)的上调和降解酶(如Pisd)的下调。
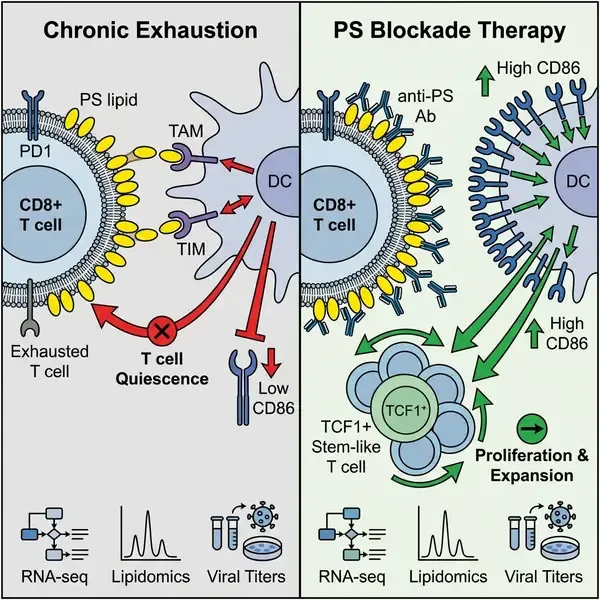
研究人员通过使用PS靶向抗体mch1N11阐明了这种“脂质翻转”的功能意义。用该抗体处理慢性感染的小鼠导致病毒特异性CD8 T细胞显著扩增,特别是TCF1+干细胞样祖细胞群体。转录谱分析显示,PS阻断使这些干细胞样细胞从其特征性的静止状态中释放出来,促进了细胞周期进入和向效应亚群的分化。从机制上讲,研究发现T细胞上外露的PS通过外源性作用抑制树突状细胞(DCs)的免疫刺激能力。通过与DCs上的PS识别受体(如TAM和TIM家族成员)结合,耗竭的T细胞限制了CD86等共刺激分子的表达。阻断这种相互作用恢复了DC的成熟,进而为T细胞的重新激活提供了必要的信号。
也许对临床转化最具意义的是,研究人员发现这种机制在人类中是保守的。来自透明细胞肾细胞癌(ccRCC)和非小细胞肺癌(NSCLC)患者的CD8肿瘤浸润淋巴细胞(TILs)在活细胞上表现出高水平的表面PS暴露。此外,研究证明了PS靶向抗体与PD-L1阻断之间具有强大的协同作用。虽然anti-PD-L1疗法主要针对T细胞内在途径,但加入PS靶向抗体解决了抑制性的髓系-T细胞轴,从而实现了更优的病毒控制和增强的效应反应。
这一发现重新定义了磷脂酰丝氨酸,它不仅是死亡的标志,更是一种动态的代谢检查点。通过确定表面脂质的外源性抑制作用,该研究为目前正在进行的将PS靶向药物(如bavituximab)与现有检查点抑制剂相结合的临床试验提供了强有力的生物学依据,可能为对抗治疗耐药性癌症和慢性感染开辟新的战线。