Androgen activity in the male embryonic hindbrain drives lethal PFA ependymoma
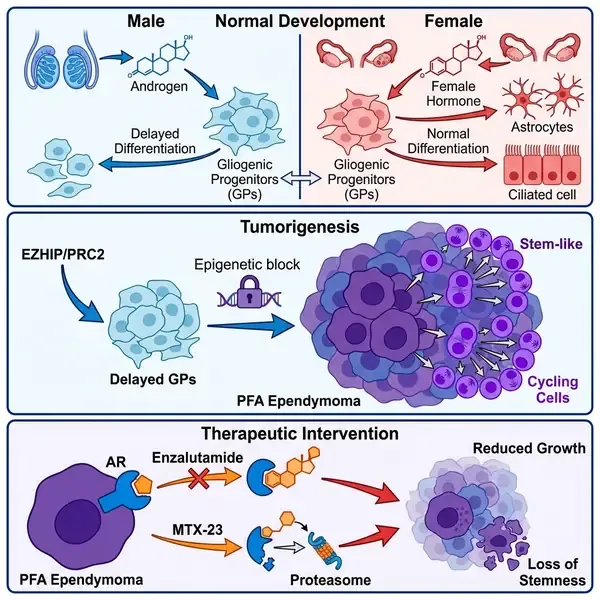
人类疾病中的性别二态性——即发病率、进展和治疗反应随生物学性别而异——仍然是肿瘤学中最深刻但研究最不充分的现象之一。在后颅窝A型(PFA)室管膜瘤中,这种差异尤为显著。这是一种致命的儿科脑肿瘤,主要影响男婴,且男孩的预后明显更差。在发表于《自然》(Nature)杂志的一项研究中,一个多学科团队为这种性别偏好提供了发育学和机制上的解释,确定了胚胎后脑中的雄激素信号是驱动肿瘤干性和致死性的主要因素。
PFA室管膜瘤具有神秘性;与大多数成人恶性肿瘤不同,它们缺乏复发性体细胞突变,似乎是由表观遗传重编程驱动的,特别是通过EZHIP蛋白抑制多梳抑制复合物2(PRC2)。虽然之前的研究集中在这些表观遗传景观上,但约1.8:1的男女发病比例的原因一直不明。通过对26个原发性PFA样本进行单细胞RNA测序(scRNA-seq),研究人员发现,男性肿瘤的特征是具有更高比例的未分化、循环的胶质生成祖细胞样(GP-like)细胞。相比之下,女性肿瘤表现出更成熟的分化层级,具有更高比例的纤毛细胞和免疫样细胞。这表明男性PFA肿瘤在发育上停滞在比女性更早、更具增殖性的阶段。
为了确定这种性别特异性的分化延迟是发育中大脑的固有属性还是肿瘤获得的特征,作者构建了跨越八个发育阶段的小鼠胚胎后脑的高分辨率转录组图谱。他们发现,即使在健康发育过程中,男性胶质生成祖细胞(GPs)的转录成熟度也低于女性同胞。男性这种发育滞后创造了一个更宽的易感时间窗,在此期间,易感祖细胞面临恶性转化的风险。
该研究最关键的机制见解来自于“四核心基因型”(FCG)小鼠模型的使用,该模型允许在实验上将性染色体(XX与XY)与性腺激素(睾丸与卵巢)解耦。结果是明确的:后脑分化的延迟是由睾丸的存在及其产生的雄激素驱动的,而不是由性染色体组决定的。无论性染色体是XX还是XY,具有睾丸的胚胎都表现出干细胞维持通路的富集和分化的抑制。相反,具有卵巢的胚胎则表现出先进的胶质生成和星形胶质细胞成熟。
在患者来源的PFA细胞系中进行的通路验证进一步巩固了雄激素受体(AR)的作用。用睾丸激素或二氢睾酮(DHT)处理显著增强了PFA细胞的克隆形成能力和生长,而雌激素或孕激素则没有这种效果。至关重要的是,这种雄激素依赖性是PFA室管膜瘤特有的;其他儿科脑肿瘤,如幕上室管膜瘤(ST-EPN)和弥漫性内源性桥脑胶质瘤(DIPG),则没有表现出这种反应。研究人员随后证明,使用临床拮抗剂恩扎卢胺(enzalutamide)或AR降解PROTAC MTX-23进行药理学阻断,能有效抑制PFA的干性和增殖。
这些发现表明,男婴体内的新生儿雄激素激增可能充当了PFA生长的“燃料”,解释了其高发病率和对现有疗法的耐药性。通过确定这种儿童癌症核心的激素依赖性发育程序,该研究开辟了一条理性的靶向治疗途径。长期作为前列腺癌治疗支柱的抗雄激素疗法,现在可能为面临这种原本无法治愈的恶性肿瘤的婴儿提供一种迫切需要的策略。