Ectopic NMDAR expression in cancer unmasks germline-encoded autoimmunity
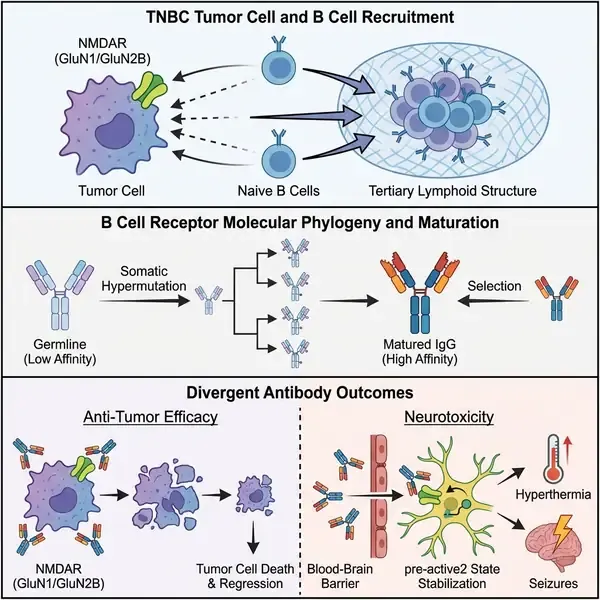
抗肿瘤免疫与自身免疫之间的生物学界限一直被视为一个连续体,但连接这两个状态的精确机制此前仍不明确。在《自然》(Nature)杂志发表的一项里程碑式研究中,研究人员阐明了三阴性乳腺癌(TNBC)中的异位蛋白表达与抗NMDA受体(NMDAR)脑炎(ANRE)发病之间的直接机制联系。通过整合空间转录组学、单细胞B细胞受体(BCR)测序和冷冻电子显微镜(cryo-EM)技术,研究团队证明了最初作为类先天免疫库一部分的生殖系编码抗体,如何在肿瘤微环境中经历亲和力成熟,从而产生既能抑制肿瘤生长又能诱发严重神经毒性的强效自身抗体。
NMDAR通常是局限于中枢神经系统的异源四聚体阳离子通道,负责介导突触可塑性。然而,该研究证实GluN1和GluN2B亚基在部分人类TNBC肿瘤中存在异位表达。利用多西环素诱导的小鼠模型(4T1-NMDAR),作者观察到这些亚基的表达足以触发强烈的适应性免疫反应。该反应的特征是B细胞被招募至肿瘤周边的三级淋巴结构,并随后产生抗NMDAR抗体。至关重要的是,高抗体滴度与肿瘤的自发消退相关,这与临床上观察到的开发出副肿瘤综合征的患者癌症预后较好的现象相吻合。
本研究的核心创新在于B细胞系统发育树的重建。研究人员将亲和力成熟的高亲和力IgG抗体追溯至其未突变的共同祖先(UCAs)。他们发现,免疫系统利用了预先存在的、对NMDAR具有基础亲和力的生殖系配置B细胞。通过肿瘤环境内的体细胞超突变和类别转换,这些“先天性”结合剂进化为高亲和力的“致病性”自身抗体。冷冻电镜结构分析显示,这些抗体主要针对NMDAR的氨基末端结构域(ATD)。结构数据表明,成熟过程涉及局部构象重排,从而稳定了抗体-受体界面,使结合亲和力提高了几个数量级。
除了单纯的结合,研究还揭示了生成的抗体之间存在复杂的效应异质性。利用双电极电压钳(TEVC)电生理技术,研究人员鉴定出一系列从强效抑制到强效增强NMDAR电流的效应。研究发现,如SK3D克隆等增强型抗体能够稳定受体一种此前未被描述的“pre-active2”构象状态。当这些增强型抗体被被动转移到健康小鼠的大脑中时,它们诱发了自主神经功能障碍(体温过高)并显著降低了癫痫发作阈值——这是ANRE的关键诊断特征。相反,抑制性抗体虽然也参与了免疫过程,但并未产生这些神经系统症状。
最后,该研究在53名TNBC患者的临床队列中验证了这些发现。约15%的患者表现出抗NMDAR抗体滴度升高,这与肿瘤内NMDAR的表达以及四年随访期内无疾病进展相关。这表明,虽然这些抗体对神经系统具有致病性,但它们也是抗肿瘤监测的强效介质。这项研究确立了免疫系统中的一种明确权衡:允许检测和破坏表达NMDAR的癌细胞的生殖系编码潜力,在成熟并进入中枢神经系统后,也为破坏性的自身免疫性疾病提供了底物。