Epigenetic memory of colitis promotes tumour growth
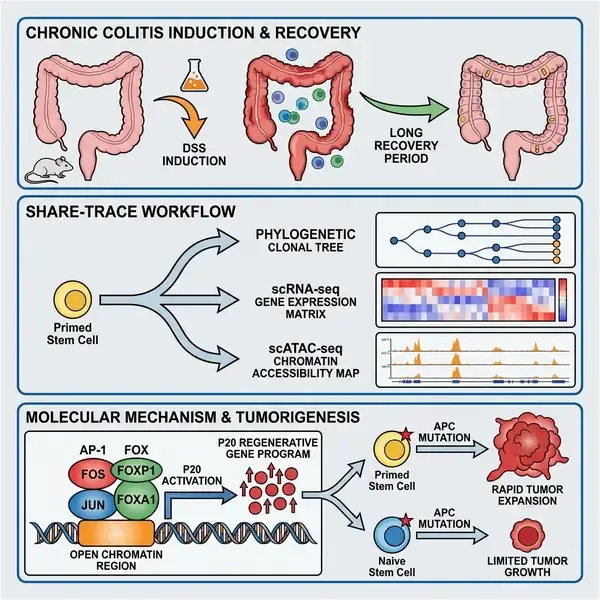
慢性炎症是公认的癌症诱因,但从炎症消退到恶性转化之间的分子桥梁一直未被完全揭示。近日,发表在《自然》(Nature)杂志上的一项研究中,Nagaraja等学者发现结肠干细胞在炎症痊愈后仍保留着持久的“表观遗传记忆”。这种分子层面的“烙印”表现为染色质可及性和转录因子动态的持久改变,在致癌突变发生时,它能显著加速肿瘤的生长。
研究团队利用右旋糖酐硫酸钠(DSS)诱导的小鼠结肠炎模型,追踪了上皮组织在急性损伤、慢性炎症及恢复期的演变。尽管在停止给药21天后,组织在形态学和转录组水平上已恢复正常,但单细胞染色质可及性测序(scATAC-seq)显示,恢复期干细胞在表观基因组上仍与对照组显著不同。最突出的特征是激活蛋白1(AP-1)基序位点的可及性累积性增加。这种表观遗传特征在炎症消退100天后(相当于经历了数十代上皮细胞更替)依然存在,表明其在再生室中具有稳定的遗传性。
该研究的一项核心技术创新是开发了SHARE-TRACE技术。这是一种单细胞多组学方法,能同时分析单个细胞的基因表达、染色质可及性和克隆演化史。通过将SHARE-TRACE应用于结肠炎恢复期组织衍生的类器官,作者证明了这种表观遗传记忆是细胞内在的,并能通过克隆谱系传递。研究发现,一类具有极高AP-1活性的特定干细胞克隆即使在缺乏外部炎症信号的情况下,仍保持着高增殖和再生的状态。这种克隆异质性表明,慢性炎症在结肠内制造了表观遗传改变的“斑块状”区域。
在机制上,研究确定了AP-1(FOS/JUN)与组织特异性叉头框(FOX)转录因子(如FOXP1和FOXA1)之间的协同作用。利用基于深度学习的足迹分析方法seq2PRINT和生化结合实验,团队证明了FOX因子能稳定AP-1在与伤口愈合和增殖相关的调控元件(P20程序)上的结合。这种协同性通过AlphaFold3结构预测以及人类炎症性肠病(IBD)样本得到了进一步验证。
研究者通过在结肠炎恢复期小鼠中诱导Apc基因缺失(结直肠癌常见的起始事件),测试了这种“表观突变”的功能后果。结果显示,这些小鼠产生的腺瘤体积明显大于对照组。至关重要的是,这种加速生长依赖于AP-1的活性;在肿瘤起始阶段使用药物抑制AP-1复合物,可将结肠炎相关肿瘤的生长限制在对照组水平。这些发现为“场癌化”(field cancerization)理论提供了有力的分子解释,即干细胞中长寿命的表观遗传改变降低了恶性转化的阈值。该研究为临床诊断和治疗开辟了新途径,提示针对炎症“记忆”的干预可能是预防慢性炎症患者发生癌症的有效策略。