Structural energetics of cold sensitivity
热敏离子通道如何将热能转化为机械门控动作,一直是感觉生物学中最具挑战性的问题之一。近日,发表在《自然》(Nature)杂志上的一项里程碑式研究,通过结合模拟原生环境的冷冻电镜(cryo-EM)技术与氢氘交换质谱(HDX–MS),为冷激活孟醇受体 TRPM8 提供了全面的结构和能量框架。这种双管齐下的方法成功捕捉到了此前未被解析的构象亚态,并定义了主导冷敏感性的热力学景观。
长期以来,TRPM8 的结构研究一直受限于使用去垢剂提取的蛋白质,这种方式往往无法保留热门控所需的微妙构象变化。为了克服这一限制,研究人员在细胞衍生囊泡中观察了人类和鸟类 TRPM8 的结构。这一方法揭示了一种全新的“半交换”(semi-swapped)架构,与大多数 TRP 通道中常见的典型结构域交换排列截然不同。在这种配置中,S6 跨膜螺旋及其相关的孔道环发生重排,与其自身的电压传感器样结构域(VSLD)结合,而不是与相邻亚基交错。这种“半交换”状态的发现表明四聚体内部存在高度动态的平衡,孔道结构域在激活过程中会发生显著的重新定位。
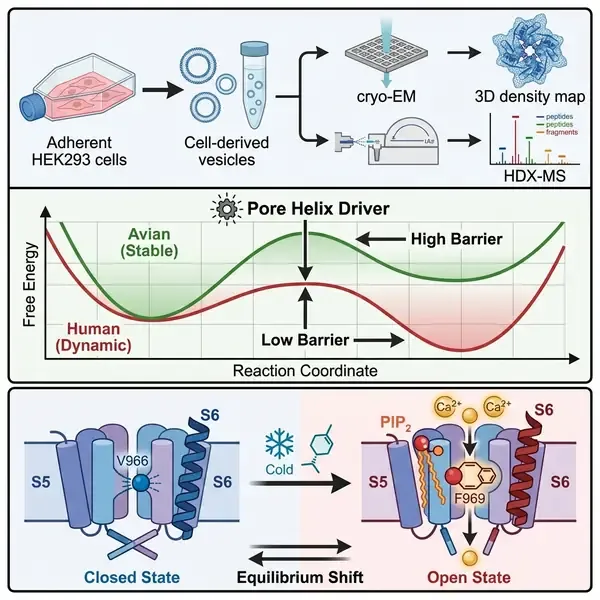
为了绘制这些转变的能量图谱,团队采用了 HDX–MS 技术,通过追踪骨架酰胺氢与溶剂氘的交换来测量蛋白质动力学。他们在孔道螺旋和 TRP 螺旋中发现了双峰质量分布,这表明存在两种缓慢互换的构象群体——即“全交换”和“半交换”状态。至关重要的是,添加孟醇或暴露于寒冷环境会将这种平衡推向“半交换”配置。通过进行温度依赖性 HDX–MS 和 van’t Hoff 分析,研究人员确定孔道螺旋是物种特异性冷敏感性的主要位点。虽然鸟类直系同源物(相对冷不敏感)在能量上保持稳定,但人类通道在激活阈值(约 26°C)附近,其孔道螺旋的标准折叠焓(ΔH°)显著下降,且局部热容(ΔCp)发生改变。
鸟类与人类通道的结构对比突出了一个关键残基——鸟类的 Y905 与哺乳动物的 V915——是这种敏感性的决定因素。在鸟类通道中,Y905 形成了一个稳定的界面,将受体锁定在关闭状态。将该残基突变为哺乳动物对应的残基(V915Y),或通过提高细胞外 pH 值来破坏该界面,可使鸟类通道对冷变得敏感。相反,哺乳动物通道缺乏这种稳定相互作用,从而拥有更宽阔的能量景观,促进了冷诱导的激活。
该研究进一步阐明了原生脂质在门控过程中的作用。冷诱导的开放结构显示,S6 螺旋的重新定位产生了一个疏水裂隙,该裂隙被内源性 PI(4,5)P2 (PIP2) 脂质的长花生四烯酰尾部占据。这种脂质结合将 S6 螺旋稳定在向上移动的 α-螺旋寄存器中,从而重新定向 F969 侧链,形成一个促进离子渗透的 π-阳离子笼。这一发现强调了 TRPM8 不仅仅是一个基于蛋白质的传感器,而是一个蛋白质-脂质复合物,其中膜环境对功能至关重要。
通过将高分辨率结构快照与残基级热力学测量相结合,这项研究首次提供了冷觉感受器运作的全景视图。它使该领域超越了静态模型,提出了一个动态自由能景观,即寒冷和化学激动剂共同作用于一个门控机制:稳定孔道螺旋并招募调节性脂质以开启离子传导通路。