Parasites trigger epithelial cell crosstalk to drive gut–brain signalling
胃肠道是一个复杂的感官界面,负责探测病原体并协调生理保护反应。虽然化学感应簇状细胞(Tuft cells)和血清素能肠嗜铬细胞(EC cells)在免疫和伤害性信号传导中的作用已被分别表征,但它们如何协作将感染信息传递给大脑的机制此前尚不明确。发表在《自然》(Nature)杂志上的一项里程碑式研究揭示了一条全新的神经免疫轴,证明了簇状细胞与EC细胞之间的旁分泌通讯在寄生虫感染期间驱动肠-脑信号传导,从而抑制摄食行为。
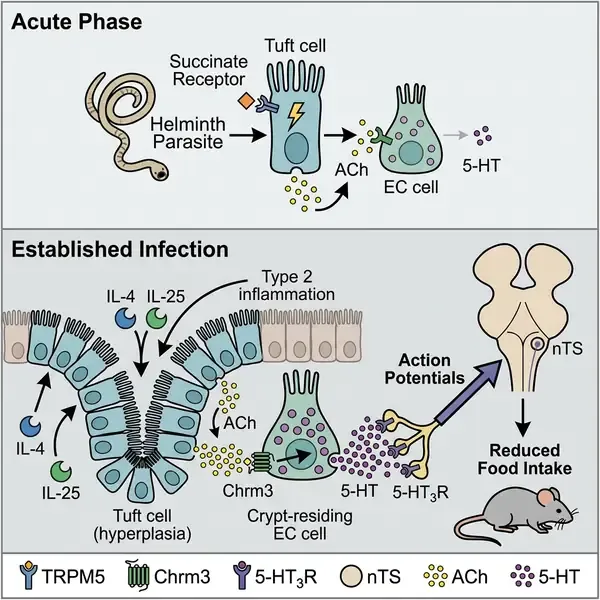
该发现的核心在于确定了一个两阶段的胆碱能-血清素能中继机制。研究发现,在蠕虫或原生动物感染期间数量激增(增生)的簇状细胞通过非传统方式释放乙酰胆碱(ACh)。尽管簇状细胞缺乏典型胆碱能神经元所具有的突触小泡和可兴奋膜,但它们利用两种截然不同的分泌模式:一种是由寄生虫代谢物(如琥珀酸)触发的、依赖于TRPM5通道的急性释放;另一种是在建立型2型炎症期间出现的持续性“渗漏样”组成型释放。这种ACh作为旁分泌信号,选择性地激活位于肠道隐窝内的EC细胞上的毒蕈碱型乙酰胆碱受体3(Chrm3)。
研究人员证实,虽然簇状细胞的急性激活提供了局部反应,但只有慢性感染特征性的持续ACh释放才能促使EC细胞释放足够水平的血清素(5-HT),从而强力刺激迷走神经传入神经元。这些表达5-HT3受体的感觉纤维将信号传递至脑干的孤束核(nTS)。通过使用PFTox小鼠(EC细胞缺乏递质释放能力)和上皮特异性ChAT缺失小鼠的功能实验,证实了这种“簇状细胞–EC细胞–迷走神经”环路是寄生虫感染高峰期观察到的厌食样摄食抑制的主要驱动力。
这项研究为寄生虫病从最初的无症状阶段进展到有症状状态提供了机械论解释。在感染早期,稀疏的簇状细胞和短暂的信号传导未能达到神经激活的阈值。然而,随着2型炎症驱动簇状细胞增生和持续的ACh分泌,由此产生的血清素激增克服了这一阈值,启动肠-脑轴以诱发保护性行为。除了直接的研究结果外,该研究还强调了肠道上皮细胞卓越的塑料性,即非兴奋性细胞可以承担类神经元的信号传导角色,从而弥合黏膜免疫系统与中枢神经系统之间的鸿沟。这些见解为管理与慢性寄生虫感染和炎症性疾病相关的胃肠道症状提供了潜在的治疗靶点。