Dominant clones leverage developmental epigenomic states to drive ependymoma
小儿癌症的分子病因学往往挑战成年肿瘤学的传统范式。成年恶性肿瘤通常源于体细胞突变的逐渐积累,而儿童肿瘤则常表现为由单一、强效的融合癌蛋白驱动的“沉默”基因组。其中,ZFTA–RELA (ZR) 融合是幕上室管膜瘤 (EPN) 的标志性特征,但该融合如何利用特定的发育窗口一直是个谜。发表在《自然》(Nature) 杂志上的一项里程碑式研究揭示,ZR 并不从头重塑表观基因组;相反,它劫持了大脑发育过程中由 PLAG/L 转录因子家族调节的预先存在的、瞬时的染色质开放程序。
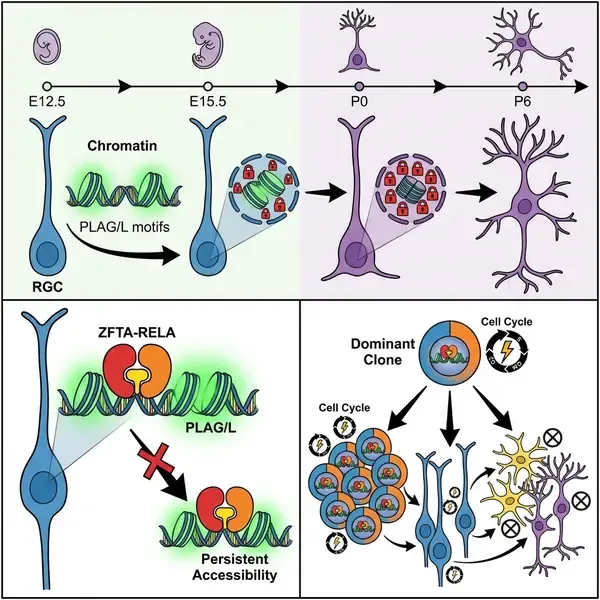
为了研究肿瘤发生与神经发育的交集,研究团队采用了单细胞核多组学 (snMultiome) 测序技术,同时捕捉了发育中的小鼠前脑和 ZR 驱动的 EPN 模型中的转录组和表观基因组图谱。研究结果表明,“处于风险中”的细胞群体是瞬时循环祖细胞,特别是放射状胶质细胞 (RGCs)。至关重要的是,研究发现,与正常细胞相比,ZR 转化的 RGCs 在全局染色质开放性模式上表现出极小的变化,尽管其癌基因靶点的转录被大量激活。这表明转化所需的染色质模块在特定的胚胎窗口期已经处于“启动”并开放的状态。
通过同源位点识别 (CSI) 测定,作者发现 ZR 融合蛋白对 PLAG/L 家族转录因子基序(特别是 GGGCC 共识序列)具有高亲和力。在正常发育中,这些 PLAG/L 基序在早期祖细胞中是开放的,但随着细胞分化为神经元或胶质细胞,它们会迅速关闭。然而,在 EPN 中,ZR 融合蛋白结合这些基序,阻止了它们的关闭,并维持了一种驱动持续增殖的类胚胎表观基因组状态。这种“表观基因组劫持”解释了为什么 ZR 融合几乎只出现在这些特定的 PLAG/L 调节模块处于活跃状态的儿童幕上肿瘤中。
除了肿瘤起始,该研究还提供了肿瘤进展的高分辨率图谱。对人类和小鼠 EPN 的跨物种分析揭示了显著的细胞异质性,反映了不完全的神经发生和胶质发生程序。通过利用 TrackerSeq(一种体内条形码技术),研究人员进行了谱系追踪,识别出优势肿瘤克隆的出现。这些单一克隆被发现能够建立肿瘤的整个细胞层级结构,从从未分化的循环祖细胞到更成熟的、有丝分裂后的神经元样和星形胶质细胞样细胞。
这一发现改变了室管膜瘤的治疗视角。观察到分化的肿瘤细胞大多不具有增殖性,这表明“分化疗法”(迫使祖细胞样细胞完成其发育程序)可能是阻止肿瘤生长的可行策略。此外,ZR 和其他靶向 PLAG/L 的融合蛋白在共享表观基因组程序上的趋同,表明 PLAG/L 顺式作用组可能是更广泛的儿科中枢神经系统恶性肿瘤的普遍弱点。通过将“发育状态”定义为融合蛋白效力的主要决定因素,这项工作为理解发育的时机和背景如何决定儿童癌症的格局提供了一个严谨的框架。