Structural basis of supercoiling-induced CRISPR–Cas9 off-target activity
CRISPR–Cas9 基因编辑的精准性常受脱靶活性的困扰,这为临床治疗应用带来了显著风险。尽管生化研究早已暗示 DNA 拓扑结构——特别是负超螺旋 ((−)SC)——会调节 Cas9 的特异性,但其分子层面的机制一直不明。近日,发表在《自然》(Nature) 杂志上的一项里程碑式研究,为理解 DNA 超螺旋如何促进脱靶识别与剪切提供了高分辨率的结构和动力学框架。
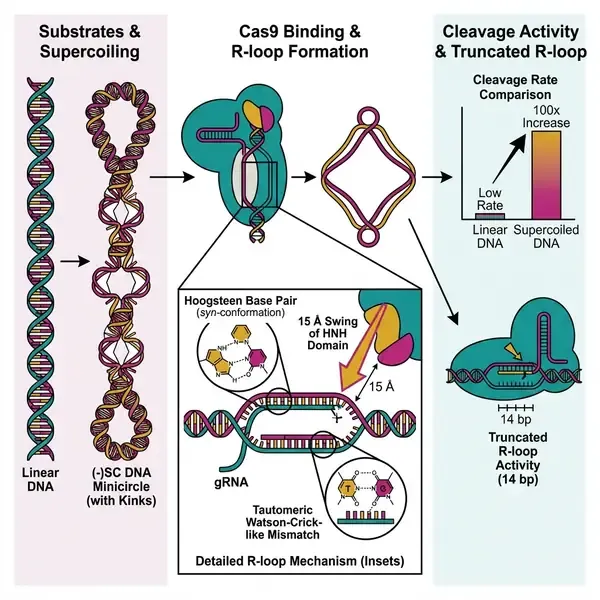
研究团队结合了冷冻电镜 (cryo-EM)、原子力显微镜 (AFM) 以及结合光镊的单分子荧光共振能量转移 (smFRET) 技术,研究了 Cas9 在负超螺旋 DNA 微环上的活性。这些 126 bp 的底物能够高度模拟真核基因组中的扭转应力。研究发现,负超螺旋 DNA 微环(天然呈塌陷或“双变性”构象)被 Cas9 剪切的速度比线性底物快 100 倍。这种增强不仅源于结合亲和力的提升,更源于酶催化状态的根本转变。
Cas9-微环复合物的冷冻电镜重构图展现了令人惊叹的“钻戒”状结构。在靶向 DNA 上,Cas9 的结合消除了超螺旋微环的结构缺陷,诱导其形成松弛的开放环状构象。至关重要的是,与之前的预催化结构相比,超螺旋复合物中的 HNH 核酸酶结构域向靶标链剪切磷酸基团摆动了 15 Å。这种“待发”状态表明,负超螺旋 DNA 中储存的扭转能降低了 HNH 结构域达到催化取向的能量势垒,从而加速了剪切反应。
该研究最深刻的见解在于脱靶识别机制。研究人员解析了 Cas9 与包含多个错配(包括种子区的关键错配)的脱靶序列(OT1 和 OT2)结合的结构。结构显示,负超螺旋 DNA 提供了必要的结构可塑性,以容纳多种非规范碱基配对几何结构。例如,第 3 位的 dG–rG 嘌呤冲突通过 DNA 碱基的 syn 构象形成的 Hoogsteen 碱基对得以解决,这一策略得益于超螺旋底物增加的灵活性。此外,研究揭示负超螺旋将剪切所需的最小 R-loop 长度从标准的 15–17 bp 降低至仅 14 bp,解释了为何在超螺旋背景下 PAM 远端错配极易被耐受。
利用光镊在扭转受限的 λ-DNA 上进行的 smFRET 动力学分析证实,当 Cas9 结合在脱靶位点时,HNH 结构域保持高度流动性,在低 FRET 和高 FRET 状态之间转换。这种灵活性受 DNA 拓扑状态的变构调节。研究还发现,即使是经过工程化改造的高保真变体(如 SuperFi 和 Sniper2L Cas9),在超螺旋底物上仍保留了显著的脱靶结合和剪切活性,凸显了克服拓扑诱导误差的挑战。
通过阐明负超螺旋如何使 HNH 结构域处于催化待发状态,并利用结构可塑性容纳错配,该研究为设计下一代 CRISPR 效应因子提供了关键蓝图。它强调了在设计用于人类基因治疗的高保真工具时,必须考虑基因组的拓扑景观,而非仅仅关注一级序列。