Pan-neurodegeneration proteomics reveals disease subtypes and molecular signatures
神经退行性疾病(NDs)长期以来主要依据临床症状和组织病理学特征进行定义,但其内在的分子异质性往往超出了这些传统分类的范畴。在一项发表于《细胞》(Cell)杂志的里程碑式研究中,一个多机构研究团队发布了泛神经退行性疾病图谱(PanNDA),这是迄今为止最全面的多层蛋白质组学框架。通过对涵盖六种主要疾病——阿尔茨海默病(AD)、路易体痴呆(LBD)、伴TDP-43病理的前额叶切迹变性(FTLD-TDP)、进行性核上性麻痹(PSP)、血管性痴呆(VAD)和帕金森病(PD)的2,279份人类大脑样本进行分析,研究人员从系统层面解析了驱动这些疾病的趋同与趋异通路。
多层蛋白质组学技术创新
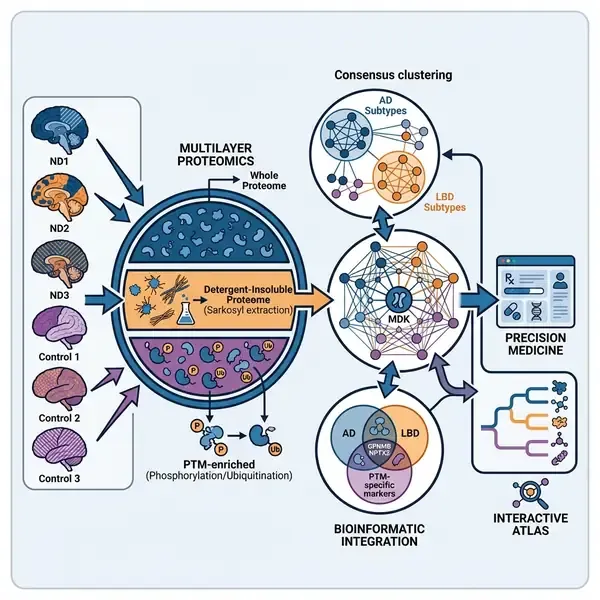
PanNDA的科学价值在于其深度多层分析方法。不同于以往仅限于全蛋白质组的研究,本研究整合了去污剂不溶性蛋白质组(捕获聚集蛋白)和翻译后修饰(PTM),特别是磷酸化和泛素化修饰。利用优化的TMT-LC/LC-MS/MS平台和创新的JUMP-ptm分析流程,团队鉴定了超过22,000种蛋白质和数千个PTM肽段。这种深度使研究人员能够超越简单的蛋白质丰度,捕获蛋白质折叠错误和酶活性变化的动态过程,而这些信息在基因组或转录组水平通常是不可见的。
重新定义疾病亚型
该研究的核心发现是在传统的疾病分类中识别出了独特的分子亚型。通过无监督共识聚类,团队将AD分为三个亚型,分别以突触信号传导、细胞骨架调节和血脑屏障(BBB)转运为特征。同样,LBD被分为四个亚型:线粒体功能、脂质代谢、转运过程和免疫炎症反应。这些蛋白质组学亚型与标准病理分级(如Braak分级)仅表现出微弱的相关性,这表明临床表现相似的患者,其背后的分子驱动因素可能存在显著差异。至关重要的是,这些亚型在独立队列中得到了验证,并可在脑脊液(CSF)中检测到,凸显了它们作为精准医疗转化生物标志物的潜力。
趋同与趋异的病理特征
通过跨疾病比较,研究识别了一组在多种NDs中共同改变的核心蛋白质。与小胶质细胞和溶酶体激活相关的GPNMB,以及参与突触调节的NPTX2,被确定为神经退行性变的通用标志物。相反,大多数差异丰度蛋白(DAPs)表现出疾病特异性,例如AD中的SPOCK2和LBD中的ATP5PO。这种分子指纹识别使得疾病间的分类具有极高的可信度,分类模型的平均AUC达到约0.9。此外,研究利用多尺度嵌入式基因共表达网络分析(MEGENA)识别了全局枢纽蛋白(GHPs)。Midkine (MDK) 被确定为AD网络中的顶级枢纽,其子网络包含APOE和APP等已知风险基因,且免疫染色证实其定位于淀粉样蛋白斑块中。
聚集蛋白的轨迹图谱
研究人员还探索了核心聚集蛋白(Aβ、pTau、SNCA、TDP-43和U1-70K)与更广泛蛋白质组之间的关系。相关性分析显示,Aβ和pTau具有重叠的蛋白质关联,表明淀粉样蛋白和tau通路存在部分趋同。相比之下,SNCA和TDP-43与截然不同的蛋白质组相关,反映了它们在突触核蛋白病和TDP-43蛋白病中的独特作用。伪时间轨迹分析进一步描绘了这些分子变化的演变过程,结果显示,虽然早期样本聚集在一起,但晚期疾病会分化为多个分子谱系,反映了神经退行性变进展过程中不断增加的异质性。
结论与资源共享
PanNDA代表了神经退行性疾病研究的基础性转变,提供了一种超越组织病理学的精细分子分类法。通过识别亚型特异性通路和关键枢纽调节因子,该研究为开发靶向疗法提供了路线图。为了确保该资源的实用性,作者推出了交互式网站(https://penglab.shinyapps.io/pannda),允许全球科学界探索这一庞大的蛋白质组学景观,加速向精准神经病学的转型。