Hyperinnervation inhibits organ-level regeneration in mammalian skin
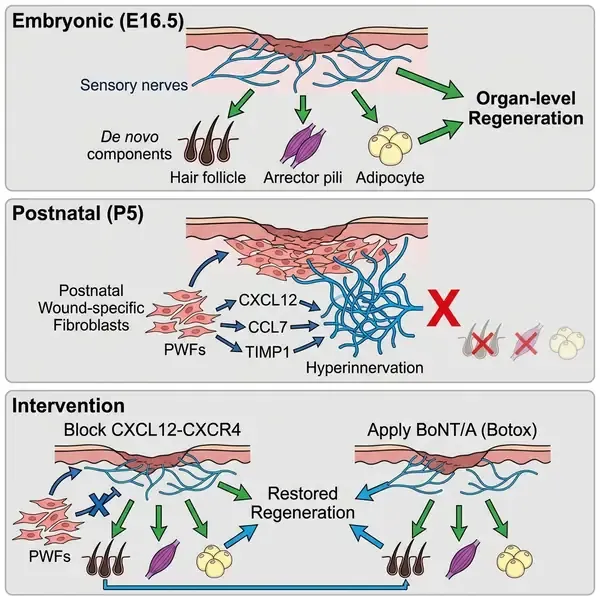
哺乳动物的器官级再生——即协调多个谱系的细胞以重建功能性器官的能力——在出生后通常会被纤维化瘢痕所取代。哈佛大学研究团队在《Cell》杂志上发表的一项里程碑式研究,成功破译了关闭哺乳动物皮肤再生窗口的分子与细胞转变机制。该研究发现,产后特有的成纤维细胞群会驱动伤口床出现“过度神经支配”(Hyperinnervation),这种过度的神经纤维萌发构成了阻碍多谱系再生的主要机械与信号屏障。
胚胎期的再生窗口
通过对比不同发育阶段的全层皮肤损伤,研究团队证实,晚期胚胎皮肤(E16.5)具有卓越的再生能力,不仅能修复表皮,还能重建包括毛囊、立毛肌(APM)、淋巴管、黑色素细胞和真皮脂肪细胞在内的全套复杂结构。至关重要的一点是,这些再生的组件在功能上是互联的;例如,再生的交感神经、立毛肌和毛囊形成了协调的单元,能够对寒冷刺激产生正常的“鸡皮疙瘩”反应。这种能力在出生后迅速下降,出生后第5天(P5)的伤口无法再生大多数谱系,转而表现为严重的瘢痕形成和过度神经支配。
产后伤口特异性成纤维细胞(PWF)的发现
利用单细胞RNA测序(scRNA-seq)技术对近9.5万个细胞进行分析,作者鉴定出了一群仅在P5损伤后出现的“产后伤口特异性成纤维细胞”(PWFs)。这些细胞极可能起源于下层皮下谱系,其特征是分泌包括CXCL12、CCL7和TIMP1在内的多种因子。为了测试这些因子的功能影响,团队在胚胎伤口中开发了一种创新的体内AAV筛选平台。他们发现,在具有再生能力的胚胎伤口中异位过表达CXCL12、CCL7或TIMP1,足以阻断多谱系再生,并诱发出产后修复特有的过度神经支配表型。
过度神经支配:再生的屏障
尽管产后伤口通常伴随炎症增加,但研究表明,髓系细胞浸润并非再生失败的决定性因素。在胚胎伤口中实验性诱导高炎症(通过LPS或细胞因子过表达)并不会阻止再生。相反,仅通过过表达神经生长因子(NGF)诱导过度神经支配,就足以完全消除胚胎皮肤的再生能力。这表明伤口床中密集、不成熟的轴突萌发是关键的抑制因素,其机制可能涉及神经递质的过度释放或对新生组织结构的物理阻碍。
开启潜在的再生潜力
该研究最重要的突破在于证实了这种再生阻碍是可逆的。通过敲除成纤维细胞来源的CXCL12或其神经元受体CXCR4,研究人员成功减少了过度神经支配,并恢复了产后小鼠的器官级再生。此外,团队还展示了利用肉毒杆菌毒素A(BoNT/A)抑制神经元囊泡释放的药理学手段,同样可以开启产后甚至成年皮肤的多谱系再生。这些发现表明,器官级再生的内在程序在发育过程中并未丢失,而是被发育成熟的周围神经系统对损伤的反应所主动抑制。这一发现为再生医学提供了全新的框架,表明通过调节神经-成纤维细胞轴,有望在人类慢性或严重创伤中恢复功能性组织结构。