STING signaling modulation by COPII cargo recognition
cGAS-STING 通路是先天免疫系统的核心哨兵,通过探测细胞质内的双链 DNA 来触发强效的炎症反应。尽管学术界早已明确 STING 必须从内质网(ER)易位至高尔基体才能启动信号传导,但控制这一“出口”过程的精确分子“通行证”一直是细胞生物学领域的一个重大空白。近日,发表在《细胞》(Cell)杂志上的一项里程碑式研究识别出了人类 STING 蛋白内部特定的内质网出口基序及其对应的 COPII 货物适配器,揭示了一种防止免疫自发过度激活的精妙调节机制。
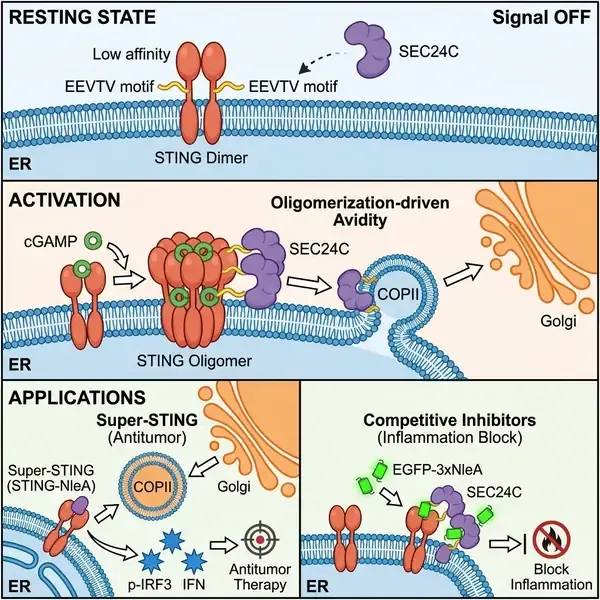
研究团队结合 CRISPR-Cas9 筛选和 AlphaFold3 结构预测技术,确定了 SEC24C 是 STING 运输所需的主要 COPII 异构体。研究精准定位了一个由五个氨基酸组成的序列——339-EEVTV-343(称为 EEΦxΦ 基序),该基序位于 STING 之前未被解析的柔性连接区。AlphaFold3 模拟显示,该基序形成了一个短的 β-折叠片,并插入 SEC24C 的 IxM 结合槽中,形成反平行的 β-折叠界面。这一发现尤为引人注目,因为 STING 的这一区域在冷冻电镜和晶体结构中通常是无序的,这凸显了下一代蛋白质折叠模型在识别瞬时但关键的信号接口方面的强大能力。
该研究的核心发现是“亲和力阈值”模型。与许多组成型离开内质网的 COPII 货物不同,STING 天然的内质网出口基序是“次优”的——它与 SEC24C 的基础亲和力较低。研究人员证实,配体诱导的寡聚化是克服这一障碍的关键。当 cGAMP 与 STING 结合时,会诱导高阶寡聚体的形成,从而增加了 EEVTV 基序的局部密度。这种聚集增强了对 SEC24C 的整体亲和力(Avidity),有效地降低了囊泡招募的阈值。该机制确保了 STING 在稳态下被隔离在内质网中,防止了强直性干扰素信号传导带来的灾难性后果。
团队进行的进化分析表明,这种 EEΦxΦ 基序在脊椎动物中高度保守。有趣的是,虽然领鞭毛虫中的 STING 同源物已经具备运输能力,但某些无脊椎动物(如海葵)缺乏这种特定基序且无法离开内质网,这表明招募 COPII 机制是 STING-干扰素轴进化过程中的关键事件。
除了基础生物学意义外,该研究还提供了极具变革性的治疗策略。通过将天然的 EEVTV 基序替换为来自细菌效应蛋白 NleA 的高亲和力序列,研究人员工程化出一种“超级内质网出口”STING 突变体。该变体绕过了对配体诱导寡聚化的需求,能够组成型地易位至高尔基体并诱导强大的抗肿瘤免疫。在小鼠模型中,诱导表达 STING-NleA 显著抑制了肿瘤生长并延长了生存期,即使在免疫缺陷背景下也是如此。相反,团队还开发了 NleA 基序的多重串联体作为竞争性抑制剂,成功阻断了内生 STING 的运输。这种双管齐下的方法——为癌症免疫治疗增强出口,为炎症性疾病阻断出口——标志着先天免疫精准调控进入了新前沿。