The E3-ome gene-centric compendium reveals the human E3 ligase landscape
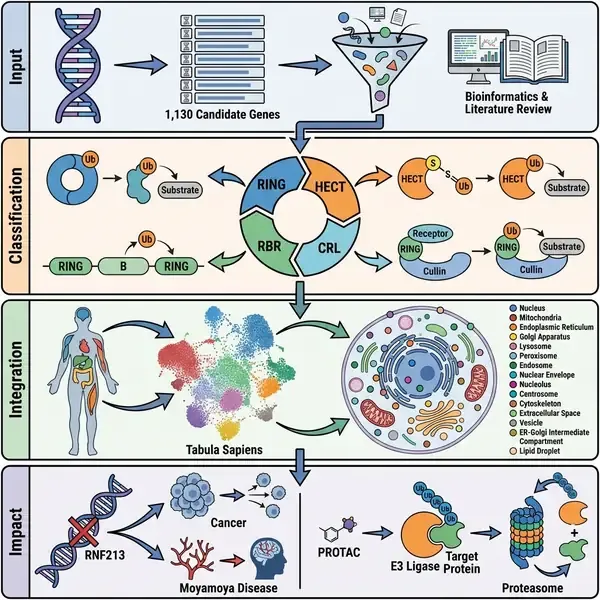
人类泛素系统的架构复杂性长期以来一直受到术语不统一和主导特异性决定因子(即 E3 泛素连接酶)目录不完整的困扰。在一项发表于《Cell》杂志的里程碑式研究中,一个国际研究联盟建立了 “E3-ome”——一个权威的、以基因为中心的人类 E3 连接酶全集,系统地分类并表征了人类 E3 连接酶的景观。通过整合实验生物化学、结构生物信息学和多尺度组学数据,该研究确定了 672 个高置信度 E3 连接酶,为机械生物学和新兴的靶向蛋白质降解领域提供了基础资源。
从历史上看,E3 连接酶(负责将泛素 [Ub] 或类泛素 [Ubl] 蛋白转移到底物的酶)一直通过不同的方法进行分类,导致文献中存在显著差异。作者通过建立统一的定义解决了这一问题:活性 E3 被定义为能够结合 E2~Ub/Ubl 中间体并催化修饰因子释放到底物或其自身的蛋白质。这一框架允许将 E3-ome 分为九个主要家族(RING、HECT、RBR、CRL1-5 和 APC/C)和两个特殊类别(退化 RING [dRING] 和非典型 E3)。值得注意的是,E3-ome 显示,在其 672 个高置信度基因中,只有 36% 与之前发布的 11 个列表共有,这凸显了此次严谨策划的变革性。
该研究的核心创新在于对 31 种人类组织、38 类细胞和 17 种细胞器的 E3 连接酶进行了多尺度图谱绘制。利用 GTEx 和 Tabula Sapiens 数据集,研究人员确定了组织偏好性表达模式,例如 PHF7 和 FBXO47 在睾丸中的富集,这两者对男性生育力至关重要。此外,通过整合全蛋白组范围的细胞器图谱,该研究将 40% 的 E3-ome 分配到了特定的亚细胞区室,发现了此前未报道的定位,包括位于中心体的 RNF213 和位于应激颗粒内的 HERC5。这种空间分辨率为理解 E3 连接酶如何维持细胞稳态提供了关键背景。
该研究还弥合了分子机制与人类病理学之间的鸿沟。遗传分析显示,26% 的 E3-ome 基因与特定的人类表型或疾病相关。其中一个突出的发现涉及 RNF213,它是全集中突变频率最高的 E3。作者在 RNF213 中发现了共同的突变,将癌症易感性与烟雾病(Moyamoya disease)联系起来,提示这些不同病理可能具有共同的分子病因。此外,研究发现 HECT E3 在孟德尔神经发育障碍(如 Angelman 综合征和 Prader-Willi 综合征)中显著富集。
在技术层面,该研究利用 AlphaFold2 结构预测和基于 DALI 的全对全结构比较来解决长期存在的注释冲突。这种方法成功地将 RING 结构域与结构相似但功能不同的 PHD 结构域区分开来。例如,G2E3 此前被错误注释为含有 PHD 的蛋白质,现已被证实拥有与 PHF7 结构类似的 RING 结构域,两者目前都被公认为 H3K14 特异性 E3。该研究还发现了新的基序,包括 FBXW5 中一个隐蔽的螺旋-环-螺旋基序,这表明它可能同时参与 CRL1 和 CRL4 复合物的形成。
总之,E3-ome 代表了我们对泛素系统理解的范式转变。通过提供标准化、高分辨率的 E3 连接酶图谱,这项工作不仅阐明了该酶类内部的进化和结构关系,还确定了大量可用于治疗性共选的未开发 E3 资源。随着制药行业寻求超越 VHL 和 CRBN 以设计 PROTAC 和分子胶,E3-ome 将成为下一代降解药物不可或缺的路线图。