Sustained nitric oxide production by engineered E. coli remodels the tumor microenvironment and potentiates immunotherapy
微生物代谢工程:持续性一氧化氮释放同步实现血管正常化与免疫重塑
癌症免疫治疗,特别是免疫检查点阻断(ICB)的疗效,常因肿瘤微环境(TME)的结构和功能病理特征而受限。TME以扭曲、渗漏的血管系统和密集的免疫抑制景观为特征,构成了限制效应T细胞浸润并促进其耗竭的物理和生物屏障。在《自然-生物技术》(Nature Biotechnology)发表的一项重大进展中,研究人员通过基因工程改造了一种益生菌株——大肠杆菌Nissle 1917(ECN),使其成为一氧化氮(NO)的局部自主生产工厂。NO是一种强效信号分子,能够同时使肿瘤血管正常化并重塑免疫环境。
构建精巧的精氨酸-一氧化氮电路
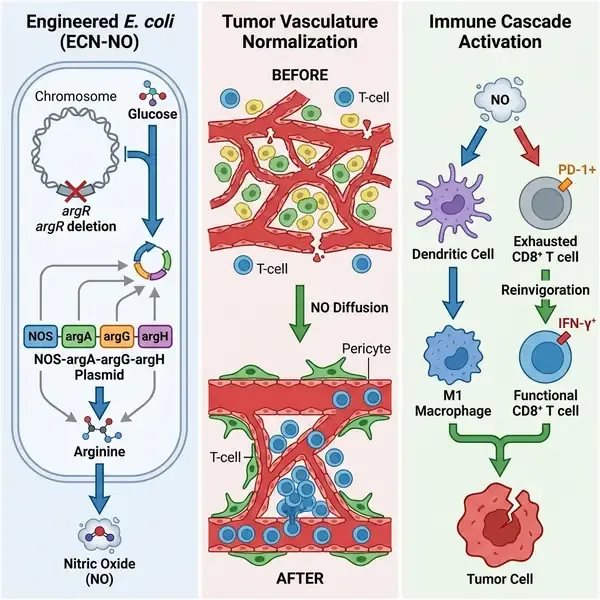
尽管已知一氧化氮具有调节血管稳态和免疫反应的作用,但其临床应用一直受限于其极短的半衰期和缺乏靶向递送系统。为了克服这些障碍,研究团队利用合成生物学技术构建了ECN-NO菌株,该菌株经过优化可实现NO的持续产生。工程化策略涉及三个关键的代谢干预:首先,删除精氨酸阻遏蛋白基因argR,以解除内源性精氨酸生物合成途径的抑制;其次,引入反馈抗性型N-乙酰谷氨酸合酶(ArgAfbr),防止高浓度精氨酸对途径的抑制;第三,将精氨酸琥珀酸合酶和裂解酶(ArgG/ArgH)与枯草芽孢杆菌一氧化氮合酶(BsNOS)共同表达。这一集成电路确保了L-精氨酸的持续供应,随后通过酶促反应转化为NO,有效地将细菌转变为自给自足的治疗引擎。
协调血管正常化
该研究最引人注目的发现之一是ECN-NO诱导肿瘤血管正常化窗口显著延长的能力。与传统的抗血管生成疗法(如VEGF抑制剂)通常导致短暂正常化后紧接着出现过度血管修剪不同,ECN-NO处理的肿瘤通过低剂量、持续释放的NO,使功能性血管系统维持了至少14天。
从机制上讲,细菌产生的NO抑制了异常的内皮细胞增殖和迁移,同时显著上调了关键的黏附分子,包括VCAM-1和ICAM-1。这种结构重塑导致周细胞覆盖率增加、血管通透性降低以及血流灌注增强。至关重要的是,这种正常化缓解了肿瘤内缺氧(免疫抑制的主要驱动因素),从而创造了一个有利于免疫细胞活动的“热”环境。
协同免疫重塑与ICB增效
研究表明,ECN-NO不仅充当血管扩张剂,还是肿瘤免疫景观的主调节因子。转录组学和单细胞RNA测序显示,ECN-NO治疗将髓系细胞群从促肿瘤(M2型)转变为促炎(M1型)表型,并减少了髓系衍生抑制细胞(MDSCs)的流行。此外,改善的血管黏附和减轻的缺氧促进了树突状细胞(DCs)的招募和成熟,这对于抗原呈递至关重要。
当与抗PD-L1(αPD-L1)疗法结合时,ECN-NO表现出卓越的治疗协同效应。在包括MC38、CT26、B16和Hepa1-6在内的多种小鼠模型中,联合疗法诱导了持久的肿瘤消退,在许多情况下实现了完全清除。这种协同作用是由功能性CD8+ T细胞的扩增和终末耗竭T细胞(PD-1+TIM-3+)的显著减少所驱动的。值得注意的是,治愈的小鼠产生了长期的免疫记忆,在超过120天的时间里能够抵抗肿瘤的再次挑战,这得到了效应和中央记忆T细胞群体增加的支持。
临床意义与生物安全性
从转化医学的角度来看,ECN-NO表现出极佳的安全性。该细菌利用TME内的缺氧和免疫特权生态位,选择性地定植于肿瘤组织,同时能迅速从肝、脾、肺等健康器官中清除。在治疗组中未观察到显著的系统毒性或体重减轻。
通过将代谢工程与功能效应物递送相结合,本研究为下一代活体生物疗法提供了坚实的蓝图。ECN-NO解决了血管功能障碍和T细胞耗竭的双重挑战,提供了一种精巧的策略,使无反应的实体瘤对免疫疗法产生敏感性。随着该领域向临床试验迈进,这一微生物平台证明了合成生物学在重塑人类疾病复杂生态系统方面的巨大潜力。