In vivo site-specific engineering to reprogram T cells
过继性细胞疗法正在经历从复杂的体外制造向直接体内工程化的范式转变。在《自然》(Nature) 杂志发表的一项里程碑式研究中,研究人员展示了一种先进的双载体系统,能够在活体生物内实现大片段 DNA 载荷在原代人 T 细胞中的位点特异性整合。这一突破解决了目前体内 CAR T 细胞生成方法的主要局限性,即通常依赖于瞬时 mRNA 表达或具有潜在风险的病毒载体随机整合。
双载体架构
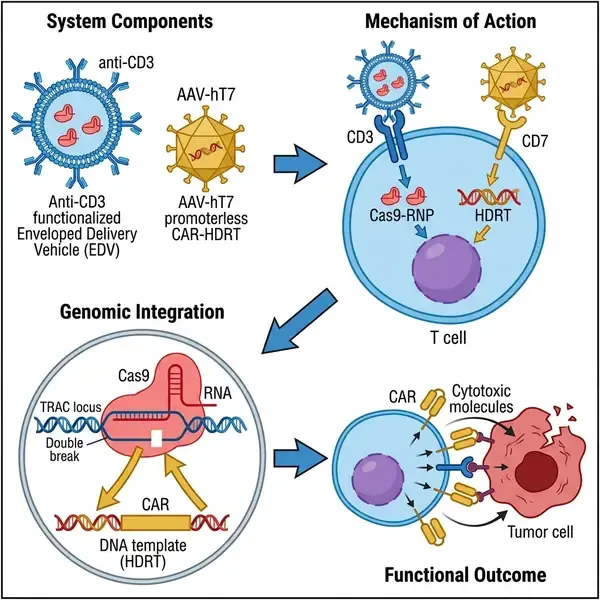
该创新的核心是一个协同递送平台,结合了包膜递送载体 (EDV) 和腺相关病毒 (AAV)。EDV 经过工程化改造,用于递送 CRISPR–Cas9 核糖核蛋白 (RNP),在人 T 细胞受体 α 恒定区 (TRAC) 位点启动双链断裂。同时,AAV 载体提供用于同源重组修复 (HDR) 的大片段 DNA 供体模板。通过靶向 TRAC 位点,研究人员确保了生成的嵌合抗原受体 (CAR) 表达受内源性 T 细胞特异性启动子的调控,从而实现生理水平的表达,并同时破坏原生 T 细胞受体——这是在异体应用中防止移植物抗宿主病的关键特征。
针对特异性和效力的工程化改造
为了将该系统转化为可行的体内疗法,团队克服了三个主要的生物学障碍:中和抗体、缺乏细胞类型特异性以及 HDR 整合所需的 T 细胞激活需求。
1. AAV-hT7 的进化:通过定向进化平台,研究人员鉴定出一种名为 AAV-hT7 的新型 AAV6 变体。该变体对人血清中和抗体表现出显著的抗性,并利用 CD7(一种泛 T 细胞标志物)作为进入细胞的主要辅助因子。 2. 靶向型 EDV:EDV 使用突变的 VSVG 蛋白进行伪分型以消除原生受体结合,并修饰了抗 CD3 单链可变片段 (scFv)。这种修饰具有双重目的:它将递送限制在 T 细胞上,并提供必要的激活信号,促使细胞进入 HDR 介导整合所需的细胞周期阶段。
跨恶性肿瘤的治疗效力
研究人员在多种人源化小鼠模型中验证了该平台。在 B 细胞急性淋巴细胞白血病 (B-ALL) 模型中,单次施用 EDV/AAV 系统即可产生治疗水平的 TRAC-CAR T 细胞,从而实现完全且持久的肿瘤缓解。值得注意的是,这种位点特异性方法优于传统的体内慢病毒载体,后者产生的 CAR 表达具有异质性且水平较低。
此外,该研究通过成功靶向用于多发性骨髓瘤的 B 细胞成熟抗原 (BCMA) 和用于实体瘤的 B7H3,展示了该平台的通用性。在 MES-SA 肉瘤模型中,体内生成的 CAR T 细胞实现了完全缓解,这标志着体内 CAR T 细胞对抗实体恶性肿瘤效力的首次证明。
科学价值与未来意义
这项研究代表了精准基因组编辑的重大飞跃。通过在体内实现位点特异性整合,该系统最大限度地降低了插入突变和抗原阴性复发的风险——这些风险通常与组成型启动子和随机整合有关。直接在患者体内重编程 T 细胞的能力可能消除昂贵的白细胞分离术和漫长的体外扩增需求,从而有望使挽救生命的 CAR T 细胞疗法更加普及。随着该领域向临床转化迈进,这种双载体策略为下一代“现货型”活体药物提供了坚实的框架。